近期,山东大学九游网页版登录入口刘新泳教授团队在国际药物化学领域顶级期刊《药物化学杂志》(Journal of Medicinal Chemistry)发表了题为“Development of Novel Dihydrofuro[3,4‑d]pyrimidine Derivatives as HIV‑1 NNRTIs to Overcome the Highly Resistant Mutant Strains F227L/V106A and K103N/Y181C”的研究成果。

获得性免疫缺陷综合征(Acquired Immunodeficiency Syndrome,AIDS),即艾滋病,是由人免疫缺陷病毒(human immunodeficiency virus,HIV)引起的严重危害全人类健康的传染性疾病。非核苷类逆转录酶抑制剂(NNRTIs)具有高效、低毒等优点,是高效抗逆转录病毒疗法(HAART)的重要组成部分。目前,已有6种NNRTIs被FDA批准,但临床上快速出现的耐药突变株(尤其是双突变株F227L/V106A以及K103N/Y181C)大大降低了它们的临床疗效。因此,亟需研发新一代新型高效抗耐药的HIV-1 NNRTIs。
近日,刘新泳团队与比利时鲁汶大学Christophe Pannecouque教授合作,设计合成了一系列二氢呋喃[3,4-d]嘧啶类NNRTIs,通过在二氢呋喃[3,4-d]嘧啶母核骨架中引入富含氢键供受体的九种不同结构的右翼,以期与RT口袋中的氨基酸残基Lys101、Lys103和Lys 104形成更强的氢键作用力。活性结果显示,化合物14b(EC50= 5.79-28.3 nM)和16c(EC50= 2.85-18.0 nM)表现出最优的抗病毒活性,尤其是对双突变株F227L/V106A和K103N/Y181C的活性均明显优于第二代上市药物依曲韦林和利匹韦林(图1)。此外,14b和16c也表现出良好的逆转录酶抑制活性(IC50= 0.14-0.15 μM),验证了该系列抑制剂的作用靶标为逆转录酶。分子对接研究探讨了化合物14b和16c与逆转录酶的相互作用,阐明了它们的抗耐药机制。其中,化合物14b是由于右翼上的甲磺酰胺与突变后的Ala106形成新的氢键作用,从而导致与HIV-1 F227L/V106A RT的结合力增加。而化合物16c由突变导致的与Cys181之间急剧减弱的π-π相互作用被广泛的氢键作用力所补偿,包括左翼的氰基乙烯基与Lys223,中心嘧啶母环上的N原子及NH linker与Lys101,以及右翼哌啶与突变后的Asn103。
此外,初步的药代动力学试验及体内安全性实验结果表明,化合物14b和16c具有良好的药代动力学性质和安全性(F= 16.6,32.1%;T1/2=1.47,1.05 h;LD50> 2000mg/kg),可作为高潜力的抗HIV-1候选药物进一步开发。
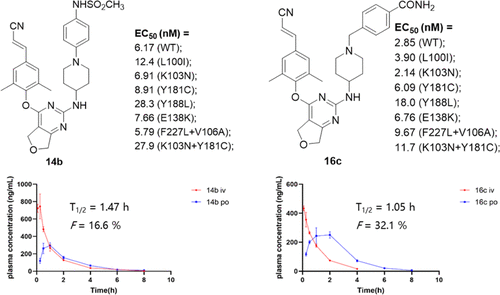
图1.候选药物14b和16c的发现
上述研究内容已发表于美国化学会药物化学领域权威期刊J Med Chem上,山东大学九游网页版登录入口康东伟研究员为论文第一作者。刘新泳教授及展鹏教授为本论文的共同通讯作者。该研究得到国家自然科学基金、山东省自然科学基金、山东省重大创新工程、山东省泰山学者计划以及齐鲁青年学者等项目的支持。
原文链接:https://doi.org/10.1021/acs.jmedchem.1c01885
